Atomaufbau im Detail - Hülle
Ah - Chemieunterricht 2005/2006 9d
s. auch Arbeitsblatt "Atomic Structure"
Experimente zur elektrostatischen Aufladung (z.B. das Reiben eines Luftballons an einem Wollpullover) zeigen, dass sich die Elektronen relativ leicht entfernen lassen. Es ist also zu vermuten, dass sich Elektronen im äußeren Bereich eines Atoms befinden - der Atomhülle.
Elektronenzahl = Protonenzahl
Die Hülle eines Atoms kann man sich in mehrere Bereiche, die kugelförmigen Schalen gegliedert vorstellen. In diesen Schalen sind die Elektronen dann in Gruppen zusammengefasst. Auf der innersten Schale, der K-Schale, können sich maximal 2 Elektronen befinden, auf der nächsten, der zweitinnersten (L-Schale), maximal 8. Auf die dritte Schale (M-Schale) kommen zunächst auch erst mal 8 Elektronen, und die nächsten Elektronen werden auf der vierten Schale (N-Schale) untergebracht (diese Regeln gelten, solange man die Elemente 1 (H, Wasserstoff) bis 20 (Ca, Calcium) betrachtet).
Bei jedem Element befinden sich in der äußersten Schale, der Valenzschale, maximal 8 Elektronen ( Oktettregel (Edelgasregel): durch Elektronenabgabe oder -aufnahme streben alle Atome eine gefüllte Außenschale an).
Schematisch sieht die Verteilung der Elektronen bei den Elementen Kalium K (19 e), Neon Ne (10 e), Silicium Si (14 e) und Bor B (5 e) wie folgt aus:
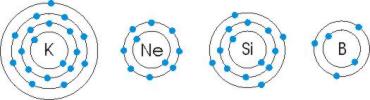
Wenn die Valenzschale gleich viele Elektronen enthält, verhalten sich chemische Elemente ähnlich.
Die Elektronen der Valenzschale lassen sich bei allen Elementen deutlich leichter entfernen als die übrigen Elektronen, die näher am Kern sind. Diese Tatsache zeigt sich auch in der Ionisierungsenergie, also der Energie, die aufgewendet werden muss, um ein Elektron abzuspalten. Jedesmal, wenn eine Schale geleert und die nächste Schale angebrochen wird, steigt die Ionisierungsenergie sprunghaft an.
Dass diese Energie für die äußeren Elektronen deutlich geringer ist als für die inneren hat zwei Gründe: zum einen kann die positive Ladung des Kerns die inneren Elektronen durch den geringeren Abstand stärker anziehen (und damit "festhalten"), zum anderen wird die Anziehungskraft der Kernladung für die äußeren Elektronen durch die dazwischenliegenden Elektronen abgeschirmt.
Bei einem Natriumatom mit 11 Elektronen, von denen 2 auf der innersten, 8 auf der mittleren und 1 Elektron auf der Valenzschale sitzen, würde man im Diagramm also nach der Entfernung des ersten und des neunten Elektrons einen deutlichen Sprung in der Stärke der Ionisierungsenergie beobachten.
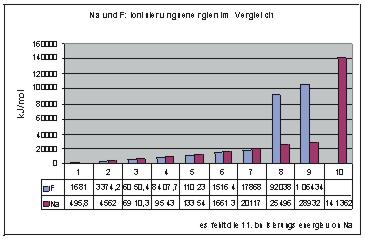
Vergleich der Ionisierungsenergien von Fluor F und Natrium Na (Werte von Wikipedia, z.B. Natrium)
Übung zum Atomkern Übung zur Atomhülle